基因编辑技术作用机制
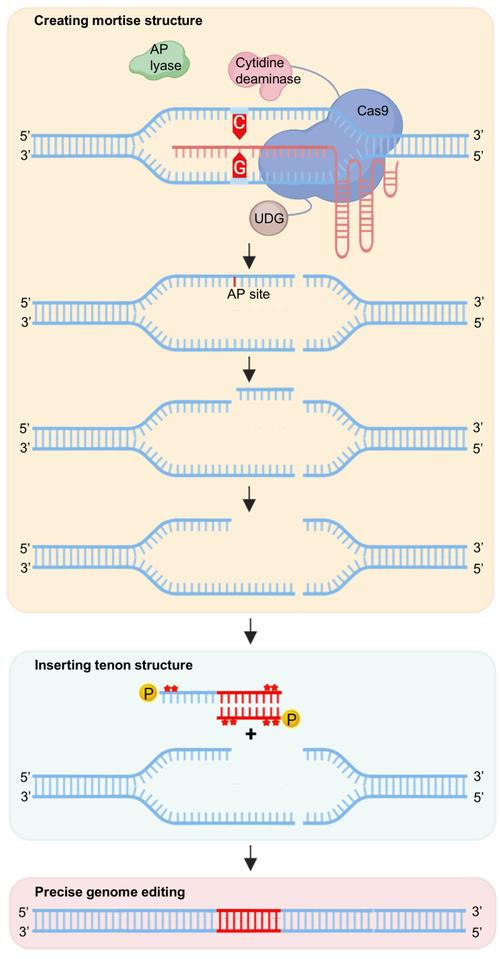
基因编辑技术是一种能够对生物体基因组特定目标基因进行修饰的基因工程技术,其核心在于通过人工设计的工具酶在DNA特定位点造成双链断裂(DSB),随后利用细胞内源性的DNA修复机制对断裂位点进行修复,从而实现对基因序列的精准修饰,目前主流的基因编辑技术包括锌指核酸酶(ZFNs)、转录激活因子样效应物核酸酶(TALENs)以及CRISPR-Cas系统,其中CRISPR-Cas9技术因操作简便、效率高、成本较低等优势,已成为当前基因编辑领域应用最广泛的技术平台。
基因编辑的作用机制主要分为三个关键步骤:靶点识别、DNA切割和DNA修复,在靶点识别阶段,编辑系统需要特异性地结合到基因组中的目标序列,对于CRISPR-Cas9系统,这一过程由向导RNA(gRNA)和Cas9蛋白共同完成,gRNA通过其5'端的20个核苷酸序列与基因组中的目标DNA序列通过碱基互补配对原则进行识别,同时需要目标位点邻近的 Protospacer Adjacent Motif(PAM)序列(如Cas9的PAM序列为NGG)的存在,以确保结合的特异性,ZFNs和TALENs则分别通过锌指蛋白(ZFP)或转录激活因子样效应物(TALE)的重复单元识别特定的DNA序列,每个重复单元通常识别3个碱基,通过组合多个重复单元实现对任意目标序列的识别。
在DNA切割阶段,不同的编辑系统利用不同的核酸酶结构域产生DNA双链断裂,Cas9蛋白含有HNH和RuvC两个核酸酶结构域,当gRNA与目标DNA结合后,HNH结构域会切割与gRNA互补的DNA链,而RuvC结构域则切割非互补链,从而形成平末端的双链断裂,ZFNs和TALENs则通过其FokI核酸酶结构域形成二聚体,每个单体结合一条DNA链,当两个单体在目标位点紧密相邻时,FokI结构域被激活,切割产生 staggered 的双链断裂(黏性末端),这种切割方式的差异会影响后续DNA修复的效率和准确性。
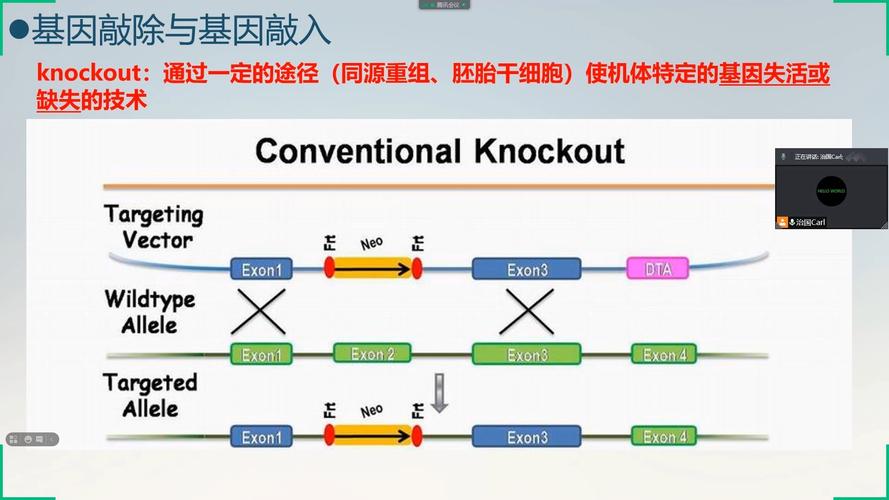
DNA修复是基因编辑实现基因修饰的核心环节,细胞主要通过两种修复机制来处理DNA双链断裂:非同源末端连接(NHEJ)和同源重组修复(HDR),NHEJ是一种直接修复机制,它将断裂的DNA末端直接连接起来,但在这个过程中常常会发生碱基的插入或缺失(Indel),导致基因 frameshift 突变或阅读框移码,从而实现基因敲除,由于NHEJ修复在细胞中占主导地位(效率较高),因此基因敲除是基因编辑最常用的应用,HDR则是一种需要模板DNA的修复机制,它以同源序列为模板,对断裂位点进行精确修复,通过设计带有特定修饰的同源修复模板(如点突变、基因插入或替换),可以实现基因的精准编辑,如基因敲入、点突变修正等,HDR修复效率较低,且主要发生在细胞周期的S期和G2期,因此在实际应用中需要通过优化实验条件(如同步化细胞、使用HDR增强剂等)来提高其效率。
除了上述基础机制,基因编辑技术还衍生出多种变体以适应不同的应用需求,Cas9蛋白的两个核酸酶结构域失活后形成Cas9 nickase(nCas9),通过设计两个相邻的gRNA,使nCas9分别在两条链上切割,从而产生定向的DSB,降低脱靶效应,碱基编辑器(Base Editor)和质粒编辑器(Prime Editor)等新型编辑工具的出现,实现了不依赖DSB的精准碱基替换和小片段插入/删除,进一步拓展了基因编辑的应用范围,碱基编辑器由失活的Cas9(dCas9)或nCas9与胞嘧啶脱氨酶或腺嘌呤脱氨酶融合而成,可以直接将C•G碱基对转换为T•A或A•T转换为G•C,无需DSB和修复模板;质粒编辑器则通过逆转录酶和逆转录模板,在gRNA引导下实现任意位点的精准编辑。
基因编辑技术的应用领域广泛,包括基础生物学研究、疾病治疗(如遗传病、癌症、传染病)、农业育种(如抗虫、抗病、高产作物培育)以及合成生物学等,该技术也面临脱靶效应、递送效率、免疫原性等挑战,需要通过优化gRNA设计、改进编辑工具蛋白、开发新型递送系统(如病毒载体、脂质纳米颗粒)等方式不断提升其安全性和有效性。
相关问答FAQs
-
基因编辑技术中的脱靶效应是什么?如何降低脱靶效应?
脱靶效应是指基因编辑工具在非目标位点进行DNA切割或修饰的现象,主要由于gRNA与基因组中非目标序列存在部分同源性或Cas9蛋白在无gRNA情况下非特异性结合导致,脱靶效应可能引起意外的基因突变,带来安全隐患,降低脱靶效应的方法包括:优化gRNA设计,选择特异性更高的gRNA序列;使用高保真Cas9变体(如SpCas9-HF1、eSpCas9);缩短gRNA长度(如17-18nt);采用双gRNA系统(如Cas9 nickase);以及开发基于结构导向的Cas9突变体等。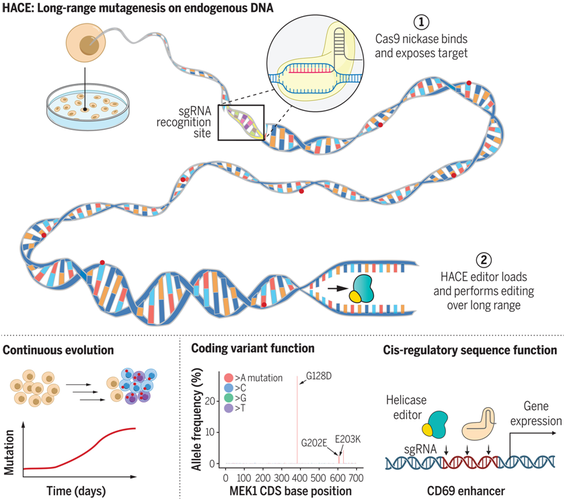 (图片来源网络,侵删)
(图片来源网络,侵删) -
基因编辑技术在临床应用中面临的主要挑战有哪些?
基因编辑技术在临床应用中面临的主要挑战包括:(1)递送效率:如何将编辑工具(如Cas9蛋白、gRNA、修复模板)高效、安全地递送至靶细胞或组织,尤其是体内递送仍存在技术瓶颈;(2)脱靶效应:如前所述,脱靶突变可能导致不可预测的后果,需通过技术手段严格控制;(3)免疫原性:Cas9蛋白来源于细菌,可能引发机体免疫反应,影响治疗效果和安全性;(4)伦理问题:对生殖细胞基因编辑的应用仍存在伦理争议,需严格遵循伦理规范;(5)长期安全性:基因编辑的长期效应尚不明确,需要更多临床数据支持。