基因编辑技术作为现代生物医学领域的前沿突破,近年来以其精准改造生物体遗传物质的能力引发了广泛关注,在众多基因编辑工具中,Ngago(NgAgo,又称NgAgo-gDNA)作为一种新型基因编辑技术,曾因其独特的机制和潜在优势备受期待,尽管其后续发展经历了争议与挑战,但仍为基因编辑技术的发展提供了重要启示,本文将围绕Ngago技术的原理、特点、研究进展、争议及应用前景展开详细阐述。
Ngago技术的核心原理与特点
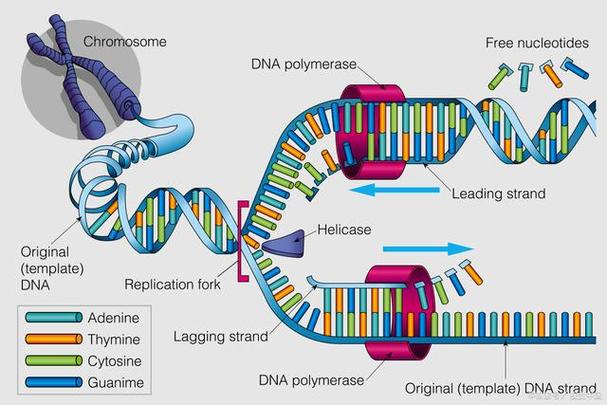
Ngago的全称为“Argonaute核酸内切酶”,是一种由细菌中的Argonaute蛋白(Ago)介导的基因编辑系统,与目前广泛应用的CRISPR-Cas9系统依赖RNA引导不同,Ngago的独特之处在于其利用DNA引导(gDNA)识别并切割目标基因,具体而言,Ngago蛋白结合一段长度约5-24个核苷酸的单链DNA(guide DNA,gDNA),形成gDNA-Ngago复合物,该复合物通过gDNA与目标DNA序列的碱基互补配对原理,识别基因组中的特定靶点,并在Ngago蛋白的催化作用下,切割目标DNA链中与gDNA互补的区域,从而实现对基因的精准修饰。
从机制上看,Ngago具有几个显著特点:一是依赖DNA引导而非RNA,理论上可避免CRISPR系统中RNA易降解导致的编辑效率波动;二是Ngago蛋白体积较小(相比Cas9蛋白),可能为病毒载体递送提供便利;三是其切割活性依赖于5'-磷酸化的gDNA,这一特性可能提高引导序列的特异性,减少脱靶效应,Ngago对目标序列的要求相对宽松,仅需满足碱基互补配对,不依赖PAM序列(Protospacer Adjacent Motif,这是CRISPR-Cas9系统识别靶点的必要序列,限制了其可编辑的靶点范围),这使其在理论上可编辑基因组中更广泛的区域。
Ngago的研究进展与争议
Ngago技术的提出可追溯至2025年,当时,中国科学家韩春雨团队在国际期刊《自然-生物技术》上发表研究,称在人类HEK293细胞和小鼠细胞中实现了Ngago介导的DNA切割,并展示了其在基因敲除、基因编辑中的高效性,这一成果迅速引发全球科学界的轰动,被认为有望超越CRISPR-Cas9成为新一代基因编辑工具。
随后的重复实验却遭遇了巨大挑战,多国实验室尝试按照韩春雨团队的方法进行实验,均未能稳定复现其结果,部分研究甚至质疑Ngago是否具有真实的基因编辑活性,2025年,《自然-生物技术》刊发“编辑关注”声明,指出该研究的重复性问题,韩春雨团队也随后补充了实验数据,但未能平息争议,2025年,该期刊最终撤回了相关论文,理由是“数据不足以支持结论”,这一事件使Ngago技术的研究陷入低谷,许多研究者转向了其他更成熟的基因编辑系统。
尽管如此,Ngago并未完全被放弃,部分学者认为,Ngago的失败可能与实验条件(如gDNA的递送效率、Ngago蛋白的表达纯化工艺等)密切相关,而非机制本身的缺陷,近年来,一些研究团队通过优化gDNA设计(如调整长度、化学修饰)、筛选更高活性的Ngago蛋白变体,或探索其在非哺乳动物系统(如细菌、植物)中的应用,试图重新激活这一技术,有研究在体外实验中证实,特定来源的Ago蛋白(如嗜热菌Ago)在高温条件下可表现出依赖gDNA的核酸酶活性,这为Ngago的机制研究提供了新线索。
Ngago的技术优势与潜在应用
尽管面临争议,Ngago在理论上仍具备独特的技术优势,若其稳定性问题得到解决,可能在多个领域展现应用潜力。
在基因治疗领域,Ngago的小分子特性使其更适合开发为体内基因编辑药物,针对单基因遗传病(如囊性纤维化、镰状细胞贫血),可通过病毒载体或脂质纳米颗粒递送Ngago蛋白和gDNA到患者靶细胞,实现对致病基因的精准修复或敲除,Ngago不依赖PAM序列的特点,使其可编辑CRISPR难以触及的基因组区域(如富含GC的序列),为治疗更多遗传疾病提供了可能。
在农业生物技术中,Ngago可用于培育抗病虫害、耐逆性强的作物品种,通过编辑植物中与病害易感性相关的基因,可减少农药使用;通过调控与干旱响应相关的基因,可提高作物在盐碱地的生长能力,由于Ngago对植物基因组编辑的效率要求相对较低,其在农作物改良中可能具有成本优势。

在基础研究领域,Ngago可作为工具基因研究基因功能,通过设计针对特定基因的gDNA,可实现对目标基因的敲除、敲入或表达调控,帮助科学家解析基因与表型的关系,Ngago依赖DNA引导的特性,也为研究DNA-蛋白质互作、DNA修复机制等提供了新模型。
Ngago面临的挑战与未来方向
当前,Ngago技术走向应用仍需克服多重挑战,首先是重复性与稳定性问题,这是其面临的核心质疑,未来研究需明确Ngago蛋白激活的关键条件(如温度、离子浓度、辅助因子等),建立标准化的实验流程,确保不同实验室可稳定复现结果,其次是递送效率,如何将Ngago蛋白和gDNA高效递送到靶细胞(尤其是体内细胞),并避免被免疫系统清除,是体内应用的关键,这可能需要开发新型递送载体(如腺相关病毒、外泌体)或对Ngago蛋白进行工程化改造(如增加细胞穿透肽)。
脱靶效应和编辑效率仍需优化,虽然Ngago理论上具有较低脱靶风险,但实际应用中仍需通过高通量测序等技术全面评估其特异性;可通过定向进化筛选更高活性的Ngago突变体,或结合gDNA的化学修饰(如硫代磷酸酯修饰)提高编辑效率。
从长远看,Ngago技术的发展需依赖多学科的交叉融合,结构生物学可通过解析Ngago-gDNA复合物的三维结构,揭示其切割机制,指导理性设计;生物信息学可帮助预测gDNA与靶位的结合效率及脱靶风险;纳米技术则可助力开发更高效的递送系统,若这些技术瓶颈得以突破,Ngago有望与CRISPR、TALENs等基因编辑技术形成互补,共同推动生物医学和农业科技的进步。
相关问答FAQs
Q1:Ngago与CRISPR-Cas9的主要区别是什么?
A:Ngago与CRISPR-Cas9的核心区别在于引导分子和识别机制,CRISPR-Cas9依赖单链RNA(sgRNA)引导识别目标DNA,且需要特定的PAM序列(如Cas9的NGG);而Ngago依赖单链DNA(gDNA)引导,无需PAM序列,理论上可编辑更广泛的基因组区域,Ngago蛋白体积小于Cas9,可能更适合体内递送,但其编辑效率和稳定性目前仍不及CRISPR-Cas9系统。
Q2:Ngago技术目前的研究现状如何?未来是否有应用前景?
A:目前Ngago技术的研究处于低谷,主要因其编辑活性的重复性未得到广泛验证,相关论文也已撤回,部分学者仍在探索其机制优化和应用潜力,如在非哺乳动物系统中验证活性、筛选高活性变体等,若其稳定性和递送效率问题得到解决,Ngago可能在基因治疗、农业育种等领域展现独特优势,但距离实际应用仍需较长时间的基础研究和技术突破。