CRISPR技术属于基因编辑技术的一种,其全称为“成簇规律间隔短回文重复序列”(Clustered Regularly Interspaced Short Palindromic Repeats),最早在1987年在大肠杆菌基因组中被偶然发现,但直到2012年,詹妮弗·杜德纳和埃马纽埃尔·卡彭蒂耶团队才阐明其作为基因编辑工具的机制,并因此获得2025年诺贝尔化学奖,CRISPR技术的核心原理是利用细菌免疫系统中的RNA引导的核酸酶系统,实现对特定DNA序列的精准切割、修饰或调控,从而在基因组水平上进行定向改造,从技术分类来看,CRISPR技术主要属于分子生物学领域的基因编辑工具,具体可归类为“第二代基因编辑技术”,与传统的TALEN(转录激活因子样效应物核酸酶)和ZFN(锌指核酸酶)相比,具有设计简单、成本较低、效率更高、可同时编辑多个位点等显著优势。
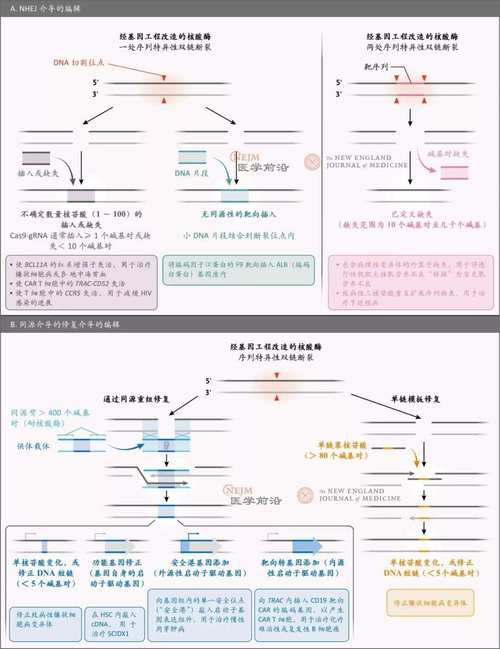
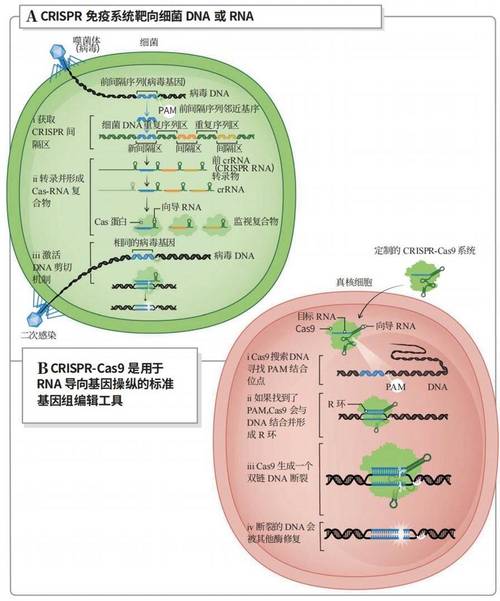
CRISPR技术的分子基础由两部分组成:一是向导RNA(guide RNA,gRNA),由CRISPR RNA(crRNA)和反式激活crRNA(tracrRNA)融合而成,负责识别并结合目标DNA序列;二是Cas蛋白(如Cas9、Cas12等),是一种核酸内切酶,在gRNA的引导下对目标DNA进行切割,根据Cas蛋白的类型和作用机制的不同,CRISPR技术可分为多个亚型,其中最常用的是CRISPR-Cas9系统,其切割目标DNA后会产生双链断裂(DSB),细胞通过非同源末端连接(NHEJ)或同源重组(HR)修复途径实现对基因的敲除、插入或替换,还有CRISPR-Cas12系统(具有切割单链DNA的活性)、CRISPR-Cas13系统(靶向RNA)等,分别应用于DNA编辑、RNA编辑和基因表达调控等领域。
从应用领域来看,CRISPR技术属于生物技术的前沿分支,广泛应用于基础研究、农业、医学、工业生物技术等多个领域,在基础研究中,CRISPR技术被用于基因功能验证、构建基因敲除或转基因模型,加速了对生命科学领域的探索;在农业领域,通过CRISPR技术可培育抗病虫害、耐逆、高产作物品种,如抗褐变的蘑菇、高产的水稻等;在医学领域,CRISPR基因疗法在遗传病治疗(如镰状细胞贫血、囊性纤维化)、癌症免疫治疗(如CAR-T细胞改造)、传染病防控(如HIV、乙型肝炎)等方面展现出巨大潜力;在工业生物技术中,CRISPR技术可用于微生物菌株改造,提高生物燃料、酶制剂等的生产效率。
从技术原理的分子机制分析,CRISPR技术属于RNA引导的靶向基因组修饰技术,其特异性识别依赖于gRNA与目标DNA序列的碱基互补配对,通常要求目标序列邻近特定的PAM序列(如Cas9的PAM为NGG),这决定了CRISPR系统的靶向精度,与传统基因编辑技术相比,CRISPR技术的核心优势在于其模块化设计——通过改变gRNA的序列即可实现对不同基因组位点的编辑,无需重新设计蛋白质结构,大大降低了技术门槛,CRISPR系统还可与多种效应蛋白融合,如转录激活因子(CRISPRa)、转录抑制因子(CRISPRi)、碱基编辑器(Base Editor)、质粒编辑器(Prime Editor)等,实现了从DNA切割到精准碱基替换、表观遗传修饰等多样化操作,扩展了其应用范围。
从技术发展阶段来看,CRISPR技术属于基因编辑领域的革命性突破,代表了从“随机突变”到“定向编辑”的技术跨越,早期的基因编辑技术(如化学诱变、辐射诱变)具有随机性和不可控性,而TALEN和ZFN虽实现了靶向编辑,但存在构建复杂、成本高昂、效率较低等问题,CRISPR技术的出现彻底改变了这一局面,使其成为目前最主流、应用最广泛的基因编辑工具,随着研究的深入,CRISPR技术不断迭代升级,如单碱基编辑技术可实现 without DSB 的精准点突变,表观遗传编辑技术可实现基因表达的精细调控,这些进展进一步巩固了CRISPR技术在生物技术领域的核心地位。
以下表格总结了CRISPR技术与其他基因编辑技术的特点对比:
| 技术类型 | 原理 | 优点 | 缺点 | 应用场景 |
|---|---|---|---|---|
| CRISPR-Cas9 | RNA引导的核酸酶切割 | 设计简单、成本低、效率高、可多靶点编辑 | 可能存在脱靶效应 | 基因敲除、插入、替换 |
| TALEN | 蛋白质-DNA识别与切割 | 特异性高 | 构建复杂、成本高、效率低 | 特定基因位点编辑 |
| ZFN | 锌指蛋白-DNA识别与切割 | 特异性较高 | 设计难度大、成本高 | 基因治疗、模型构建 |
| 碱基编辑器 | 脱氨酶与Cas蛋白融合 | 无DSB、精准点突变 | 窗口限制、可能产生副产物 | 单基因遗传病治疗 |
| 表观遗传编辑器 | Cas蛋白与效应结构域融合 | 可逆调控基因表达 | 效率较低、持续时间有限 | 基因功能研究、疾病治疗 |
尽管CRISPR技术具有广泛的应用前景,但其安全性、伦理问题仍需关注,脱靶效应可能导致非预期基因突变,生殖细胞编辑可能引发遗传改变传递给后代,因此目前大多数临床研究仅限于体细胞编辑,全球范围内对CRISPR技术的监管政策尚不统一,如何平衡技术创新与伦理规范成为重要课题。
相关问答FAQs:
-
问:CRISPR技术与传统基因编辑技术(如TALEN、ZFN)的主要区别是什么?
答:CRISPR技术与传统技术的核心区别在于靶向机制和构建难度,TALEN和ZFN依赖于蛋白质-DNA识别,需要针对每个目标位点设计特定的蛋白质结构,构建复杂且成本高昂;而CRISPR技术通过RNA引导靶向,仅需设计gRNA序列即可实现不同位点的编辑,具有设计简单、成本低、效率高、可同时编辑多个位点等优势,CRISPR技术的脱靶效应相对可控,且可通过优化gRNA设计和Cas蛋白变体(如高保真Cas9)进一步降低。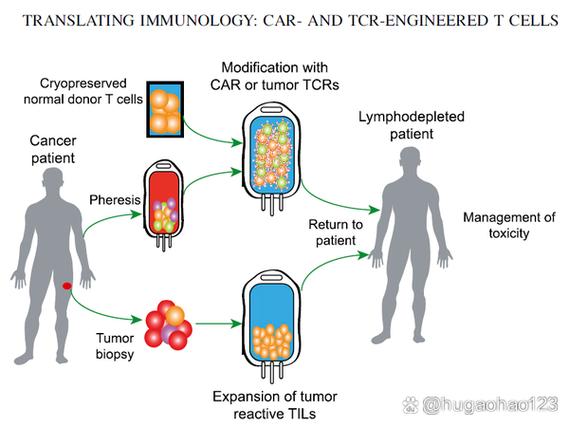 (图片来源网络,侵删)
(图片来源网络,侵删) -
问:CRISPR技术在医学领域面临的主要挑战有哪些?
答:CRISPR技术在医学应用中面临多重挑战:一是脱靶效应,可能导致非预期基因突变,引发安全问题;二是递送系统,如何将CRISPR组件精准递送至靶组织或细胞(如肝脏、大脑)仍是技术瓶颈;三是免疫原性,Cas蛋白可能引发机体免疫反应,影响治疗效果;四是伦理争议,尤其是生殖细胞编辑涉及后代基因改变,存在伦理和法律风险,研究人员正通过开发高保真Cas蛋白、优化递送载体(如病毒载体、脂质纳米颗粒)以及建立严格的评估体系来应对这些挑战。